近日,在美国达拉斯举行的美国泌尿肿瘤学会(SUO)年会上,UroGen Pharma公司公布了3期ENVISION试验的积极结果:前沿药UGN-102治疗低级别、中风险非肌层浸润性膀胱癌(LG-IR-NMIBC),显示出令人鼓舞的疗效,患者的复发率显著降低,并且疗效持久。
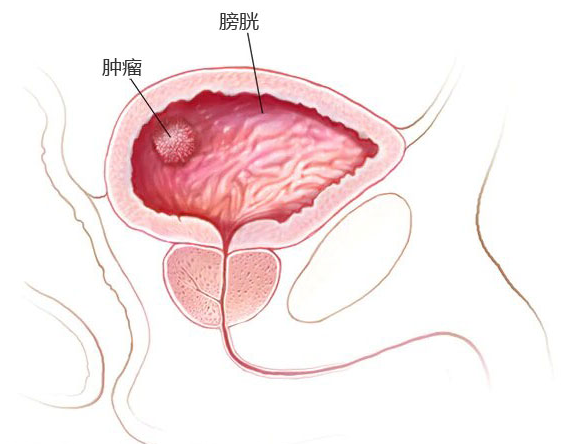
非肌层浸润性膀胱癌(NMIBC)的标准治疗方法是经尿道膀胱肿瘤切除术(TURBT)。多达70%的NMIBC患者会经历至少一次复发,而低级别、中风险非肌层浸润性膀胱癌(LG-IR-NMIBC)患者更容易复发,并且需要接受多次TURBT手术。
什么是UGN-102?
UGN-102是一种创新的膀胱内注射药物,主要活性成分是化疗药丝裂霉素,它采用了UroGen公司独有的RTGel技术,这是一种基于水凝胶的持续释放配方,能将丝裂霉素包裹在水凝胶中,并在膀胱内缓慢释放。通过这种方式,能更有效地作用于膀胱肿瘤。
UGN-102目前正在进行3期临床试验,用于治疗低级别、中风险非肌层浸润性膀胱癌(LG-IR-NMIBC)。
UroGen公司已于2024年8月向美国食品药品监督管理局(FDA)提交了新药申请(NDA),FDA预计将在2025年6月13日前做出审批决定。
UGN-102相关临床试验:
ENVISION试验是一项单臂、多国、多中心的3期研究,旨在评估UGN-102治疗低级别、中风险非肌层浸润性膀胱癌(LG-IR-NMIBC)患者的疗效和安全性。
ENVISION试验已完成目标入组,共招募约240名患者,分布在56个研究中心。
研究参与者接受了6次UGN-102(每周一次)膀胱内灌注治疗。
该研究的主要终点为治疗后3个月的完全缓解率。
关键的次要终点为3个月获得完全缓解的患者的持续反应时间。
研究结果:
在使用UGN-102治疗的患者中,经过3个月的治疗后,获得完全缓解(即肿瘤完全消失)的患者,在接下来的12个月里,有82.3%的患者仍保持完全缓解的状态。
根据估算,接下来15个月和18个月时,这种趋势仍势头强劲,有80.9%的患者仍保持完全缓解的状态。
这些结果进一步支持了试验的主要终点,即接受UGN-102初次治疗后3个月的完全缓解率为79.6%。
安全性:
ENVISION试验中观察到的蕞常见的治疗相关不良事件(TEAE)包括排尿痛、血尿、尿路感染、尿频、疲劳和尿潴留(指尿液无法正常排出,导致膀胱内尿液积聚的情况)。
TEAE通常为轻度至中度,且多数已解决或正在解决。
ENVISION试验的安全性数据与之前的临床试验一致,进一步支持其作为低级别、中风险非肌层浸润性膀胱癌(LG-IR-NMIBC)患者新治疗选择的潜力。