概述:
据悉,前沿药UGN-102在低级别中度风险非肌层浸润性膀胱癌患者中表现出令人鼓舞的疗效。
UGN-102由UroGen Pharma公司研究,UroGen Pharma公司是一家跨国制药公司,刚开始在以色列成立,目前总部位于美国新泽西州普林斯顿。UGN-102是一种创新的膀胱内注射药物,主要活性成分是化疗药丝裂霉素。
目前,UGN-102正在接受美国食品药品监督管理局(FDA)对该适应症的审查。
FDA已于2024年10月接受了UGN-102的新药申请(NDA),预计将于2025年6月13日做出审批决定。
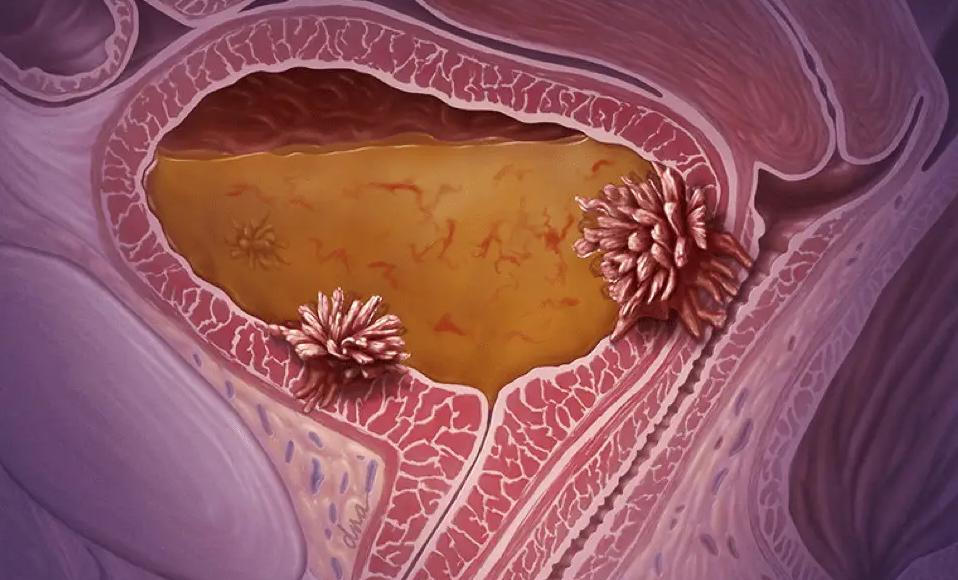
相关数据:
ENVISION试验(NCT05243550)是一项来自多国的单臂试验,评估了UGN-102作为主要化学消融疗法,在复发性低级别中度风险非肌层浸润性膀胱癌患者中的疗效和安全性。共有240名患者参与试验,接受了UGN-102膀胱内灌注治疗,每次通过尿道导管进行75毫克、总计6次、每周一次的灌注治疗。
该试验的主要终点是3个月时的完全缓解(CR)率。次要终点包括在3个月时达到完全缓解的患者的缓解持续时间(DOR)、持久的完全缓解率、3个月时达到完全缓解的患者的无病生存率以及安全性。
根据3期ENVISION试验的研究数据,治疗3个月达到完全缓解(CR)的患者,即肿瘤完全消失的患者:
18个月的无进展生存率为80.6%,意味着有80.6%的患者在18个月内持续保持完全缓解(肿瘤完全消失)状态。
12个月的无进展生存率为82.5%,意味着有82.5%的患者在12个月内持续保持完全缓解(肿瘤完全消失)状态。
在安全性方面,治疗相关的不良事件(TEAEs)包括排尿困难(23.0%)、血尿(8.3%)、尿路感染(7.1%)、多尿(6.7%)、疲劳(5.4%)、尿潴留(5.0%)、尿道狭窄(4.6%)、新冠(3.8%)、便秘(3.8%)、恶心(3.8%)和排尿急迫(3.8%)。
来源:
https://www.cancernetwork.com/view/ugn-102-yields-enduring-18-month-responses-in-low-grade-nmibc